Burkholderia pseudomallei est une bactérie à Gram négatif, présente dans le sol et l’eau de pays tropicaux et subtropicaux. En outre, des infections d’origine locale ont récemment été recensées aux États-Unis.
La mélioïdose, la maladie clinique causée par B. pseudomallei, devrait être recherchée chez les personnes de retour d’une région endémique, qui présentent de la fièvre et une pneumonie, ou un abcès au foie, à la rate ou à la prostate, ou encore une arthrite septique.
Burkholderia pseudomallei peut être difficile à identifier avec les techniques de microbiologie classiques.
Les laboratoires de microbiologie devraient être avisés de la présomption diagnostique afin de prévenir l’exposition accidentelle du personnel.
Une femme de 64 ans s’est présentée aux services des urgences d’un hôpital de Toronto (Ontario) en raison d’une douleur à la cheville gauche et de fièvre, apparues 3 jours plus tôt. Elle avait des antécédents de diabète, d’hypertension et de purpura thrombopénique immunologique. Ses médicaments étaient les suivants: metformine, sitagliptine, canagliflozine, gliclazide, amlodipine et telmisartan. Six semaines auparavant, elle était rentrée de Puri, en Inde, où elle avait passé l’hiver à rendre visite à des membres de sa famille et avait marché pieds nus dans les eaux saumâtres du lac Chilika.
À l’examen, la température s’élevait à 39,4 °C et la cheville gauche était enflée, chaude et sensible. Les premières analyses de laboratoire d’intérêt comprenaient une leucocytémie normale, un taux d’hémoglobine de 123 g/L (plage normale 137–180 g/L) et un taux élevé de protéine C réactive de 30 mg/L (plage normale 0–8 mg/L). Les hémocultures étaient négatives. Une radiographie de la cheville a mis en évidence une enflure diffuse des tissus mous. L’urgentiste a demandé une consultation en chirurgie orthopédique, après quoi une ponction articulaire a été réalisée et a permis de prélever 3 mL de liquide sanguinolent. La coloration de Gram du prélèvement a montré l’absence de micro-organismes et une numération leucocytaire polymorphonucléaire modérée; la culture était négative. Dans le cadre de la prise en charge empirique de l’arthrite septique, il y a eu administration de céfazoline, sélectionnée pour cibler le staphylocoque doré sensible à la méthicilline.
La patiente a été hospitalisée afin de permettre la poursuite du traitement et de l’observation. La douleur à la cheville gauche et la fièvre persistaient. Compte tenu de son séjour récent en Inde, nous avons réalisé d’autres analyses. Les frottis sanguins par étalement mince et goutte épaisse ont exclu le diagnostic de paludisme; les analyses sérologiques du dépistage du VIH, de la syphilis, de Bartonella, de Brucella et de la fièvre Q étaient négatives, de même que les coprocultures à la recherche de bactéries, d’œufs et de parasites. L’imagerie par résonance magnétique (IRM) de la cheville a révélé un léger épanchement tibio-talaire et un œdème sous-cutané. Comme ces résultats n’évoquaient pas l’arthrite septique, l’équipe d’orthopédie a jugé que le drainage chirurgical n’était pas nécessaire.
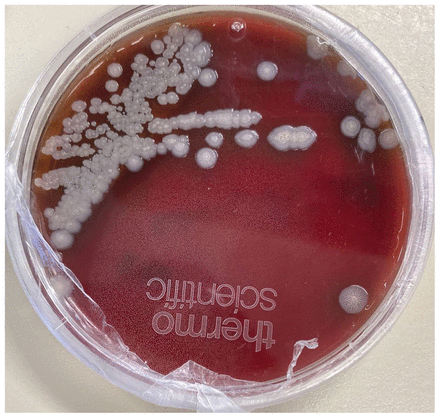
La patiente avait encore de la fièvre et de la douleur. Dix jours après la consultation initiale, une deuxième ponction articulaire a eu lieu en radiologie interventionnelle; 2 mL de pus ont été prélevés. Aucun micro-organisme n’était visible à la coloration de Gram, mais on a observé la croissance de colonies lisses et grises sur gélose au sang après 24 heures d’incubation (figure 1). Il y a donc eu analyse de la colonie par spectrométrie de masse à temps de vol après désorption/ionisation laser assistée par matrice (MALDI-TOF) (Bruker MALDI Biotyper). Le meilleur appariement était Burkholderia thailandensis, avec un score de 1,9, ce qui semblait indiquer une mauvaise identification potentielle de l’espèce; un score compris entre 1,7 et 1,99 permet d’identifier le genre du micro-organisme et un score de 2–3, l’espèce. En raison de ce résultat, l’équipe de microbiologie médicale a commandé un test de réaction en chaîne par polymérase (RCP) au laboratoire de Santé publique Ontario et au Laboratoire national de microbiologie, qui ont identifié cet isolat comme B. pseudomallei. L’antibiogramme a montré que ce dernier était sensible à la ceftazidime, à l’imipénem, au triméthoprime–sulfaméthoxazole, à l’amoxicilline–acide clavulanique et à la doxycycline.
Croissance de Burkholderia pseudomallei sur gélose au sang, après une période d’incubation de 24 heures du liquide prélevé dans la cheville d’une femme de 64 ans ayant une douleur à la cheville et de la fièvre depuis 3 jours, 6 semaines après avoir voyagé en Inde.
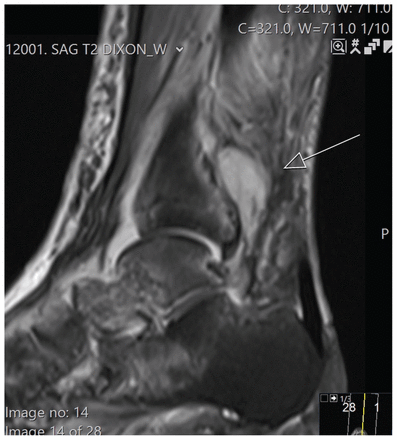
Sur la base des résultats d’analyse, un diagnostic de mélioïdose a été posé. Nous avons remplacé l’antibiothérapie par du triméthoprime–sulfaméthoxazole et du méropénem, ce qui a fait tomber la fièvre. À l’arrivée des résultats de l’antibiogramme, le méropénem a été substitué à la ceftazidime. La douleur étant toujours présente, la patiente a passé une deuxième IRM, qui a montré une progression depuis la précédente, avec des signes d’arthrite septique se manifestant par un abcès à l’arrière du tibia distal, une ostéomyélite de la mortaise de la cheville et de petits abcès sous-cutanés (figure 2). La radiographie thoracique n’a pas révélé d’atteinte pulmonaire.
Imagerie par résonance magnétique de la cheville: vue sagittale avec pondération en T2 montrant des signes évocateurs d’abcès avec signal élevé (flèche), postérieur au tibia distal.
Deux semaines après son hospitalisation, la patiente a subi une arthrotomie avec irrigation et débridement de la cheville. Elle a reçu 500 mg de méropénem intraveineux, toutes les 6 heures, pendant 2 semaines, puis 2 g de ceftazidime, toutes les 6 heures, pendant 6 semaines, en association, pour les 2 schémas, avec 2 comprimés à double dose de triméthoprime–sulfaméthoxazole, 2 fois par jour. À l’issue du traitement à la ceftazidime, elle a poursuivi la prise de triméthoprime–sulfaméthoxazole, par voie orale, en monothérapie, à la même dose, pendant 2 mois. Des examens ont révélé la présence de thrombopénie (le taux de plaquettes était inférieur à 50 au moment de l’hospitalisation, mais la valeur de référence variait entre 100 et la plage normale), ce qui a fait soupçonner une réaction indésirable au triméthoprime–sulfaméthoxazole; nous lui avons donc prescrit 100 mg de doxycycline, par voie orale, 2 fois par jour, pour terminer une cure de 6 mois. Au moment du rendez-vous de suivi, 4 mois après son opération, elle avait une douleur résiduelle et marchait sans assistance.
Au cours de ce cas, 3 technologues ont été exposés accidentellement à la bactérie pendant les analyses courantes sur une paillasse à découvert. L’équipe de médecine du travail a jugé le risque faible et n’a donc pas recommandé de prophylaxie, mais a demandé aux personnes concernées de surveiller l’apparition de symptômes. Une demande d’analyse sérologique de référence pour le dépistage de B. pseudomallei a été envoyée aux Centers for Disease Control and Prevention des États-Unis, suivie d’une sérologie de convalescence 6 semaines plus tard pour évaluation de la séroconversion.
Discussion
Épidémiologie de Burkholderia pseudomallei
La mélioïdose est la maladie clinique causée par B. pseudomallei, un micro-organisme présent dans les régions tropicales et subtropicales, en particulier en Asie du Sud-Est — la plus grande incidence déclarée est en Thaïlande — ainsi qu’au nord de l’Australie et dans le sous-continent indien. Selon des rapports, on observe une transmission endémique émergente de la maladie au Brésil et en Afrique équatoriale1. Des infections d’origine locale ont été contractées aux États-Unis après des expositions au sol, dans les États du golfe du Mexique, ainsi qu’à des produits d’aromathérapie importés2. Le caractère endémique de cette dissémination fait l’objet de nombreuses études et pourrait être lié aux changements climatiques1. On estime que 165 000 cas de mélioïdose sont recensés chaque année, dans le monde, mais le sous-diagnostic et la sousdéclaration de la maladie constituent un problème important3.
Dans les régions endémiques, où les bactéries sont omniprésentes dans l’eau et dans le sol, la transmission se produit surtout pendant la saison des fortes pluies3. Burkholderia pseudomallei est capable de survivre pendant des années dans les milieux humides. La contamination se fait par contact avec une lésion cutanée, par inhalation ou par ingestion. La transmission interpersonnelle étant rare, aucune mesure d’isolement n’est nécessaire pour les personnes infectées. Afin d’éviter l’exposition à la bactérie en région endémique, il est conseillé de bouillir l’eau avant de la boire et de porter des chaussures pendant les travaux agricoles ou des visites lorsqu’un contact direct avec le sol ou l’eau est nécessaire3.
Parmi les adultes qui contractent la maladie clinique, 80 % souffrent d’affections concomitantes, dont le diabète mellitus, une hépatopathie ou une néphropathie chroniques, l’alcoolisme ou une immunosuppression d’origine médicamenteuse ou pathologique4,5.
Tableau clinique de la mélioïdose et diagnostic différentiel de l’arthrite septique
La période d’incubation de B. pseudomallei dure 9 jours en moyenne. Tout comme la tuberculose, B. pseudomallei a été qualifié de « grand imitateur » en raison de ses nombreuses manifestations et de sa longue période de latence qui peut durer des mois, voire des années, avant l’apparition d’une infection symptomatique4. La mortalité s’élève à 40 % dans certaines régions endémiques où l’accès précoce aux soins intensifs est restreint. Un choc septique est possible dans 20 % des cas3,5.
La mélioïdose se présente comme un syndrome fébrile. La manifestation la plus fréquente est la pneumonie aiguë, qui peut dégénérer en abcès pulmonaires et en empyème. L’infection peut se propager et entraîner des abcès au foie, à la rate, au rein ou à la prostate. La propagation aux os et aux articulations, à l’origine de l’ostéomyélite et de l’arthrite septique, se produit dans 10 % des cas3. Les abcès parotidiens sont une manifestation fréquente chez l’enfant. Rares, les manifestations touchant le système nerveux central comprennent les abcès cérébraux et l’encéphalomyélite. L’infection cutanée locale peut entraîner une ulcération ou des abcès sous-cutanés3.
L’arthrite septique se présente comme une monoarthrite aiguë6. Le diagnostic est posé en cas de ponction de liquide articulaire révélant une leucocytose généralement supérieure à 50 000/mm3 et de culture bactérienne positive. La coloration de Gram oriente le traitement empirique6. Le staphylocoque doré est la cause d’arthrite septique la plus fréquente dans le monde, ce qui représente de 35 %–65 % des cas. Il faut aussi rechercher les streptocoques, l’arthrite gonococcique et, même s’ils sont plus rares, les bacilles à Gram négatif7. Les antécédents de voyage devraient être relevés systématiquement en cas de fièvre et d’arthrite septique afin que soit envisagée la possibilité de maladies infectieuses non présentes localement (tableau 1).
Considérations diagnostiques et microbiologiques
Burkholderia pseudomallei est un bacille à Gram négatif, aérobie, ne formant pas de spores8. La bactérie se multiplie facilement sur les géloses d’utilisation courante dans les laboratoires pour la culture bactérienne des spécimens liquidiens et tissulaires. Il peut toutefois être très difficile de distinguer B. pseudomallei d’autres espèces du genre Burkholderia8. Dans la plupart des laboratoires de microbiologie, la spectrométrie de masse MALDITOF est le principal outil d’identification des micro-organismes isolés à partir de spécimens cliniques, mais B. pseudomallei ne figure pas dans la base de données commerciale du spectromètre de masse MALDI-TOF de Bruker. L’isolat de la patiente a été envoyé à des laboratoires de référence, qui ont réalisé une RCP multiplex pour identifier définitivement B. pseudomallei.
Pour le diagnostic, il faut réaliser des hémocultures, en plus de cultures de tous les sites suspects. Plusieurs spécimens doivent être prélevés afin d’améliorer le rendement, puisque l’hémoculture a une sensibilité de 50 % seulement3. Comme B. pseudomallei n’est pas colonisateur, l’isolement d’un seul site permet le diagnostic de la mélioïdose5. La culture reste la méthode diagnostique de référence5. La sérologie n’est généralement pas utilisée pour confirmer le diagnostic puisqu’elle ne distingue pas l’infection aiguë des infections antérieures5.
Burkholderia pseudomallei est un agent hautement pathogène du groupe de risque 3, c’est-à-dire qu’il pose un risque infectieux important pour le personnel du laboratoire de microbiologie. Pour prévenir l’exposition, les technologues doivent porter un équipement de protection individuelle adapté et manipuler la culture dans une enceinte de sécurité biologique de catégorie II. Une exposition accidentelle en laboratoire peut survenir en cas d’inhalation d’aérosols infectieux ou de contact avec une lésion cutanée. Si la présence de la bactérie est soupçonnée, les cliniciens devraient donc aviser le laboratoire avant de lui adresser les spécimens cliniques. La prophylaxie peut s’imposer après une exposition en laboratoire, en fonction du niveau de risque d’exposition et de la présence de maladies ou d’états concomitants comme la grossesse, le diabète et l’immunodépression. La prise de triméthoprime–sulfaméthoxazole ou de doxycycline pendant 21 jours, amorcée dans les 24 heures suivant l’exposition, est la mesure de prophylaxie postexposition privilégiée, mais son efficacité n’est pas établie9. La maladie due à B. pseudomallei peut être difficile à repérer en raison du potentiel d’infection latente. L’analyse sérologique de B. pseudomalle en phase aiguë et de convalescence permet de surveiller la séroconversion après une exposition9.
Prise en charge
L’amorce rapide d’une antibiothérapie intraveineuse et la réanimation sont cruciales en cas de sepsie. Burkholderia pseudomallei est intrinsèquement résistant à la pénicilline, à la céphalosporine de première et seconde génération, et aux aminosides5. La plupart des isolats sont sensibles à la ceftazidime, au méropénem, à l’imipénem et à l’amoxicilline–acide clavulanique.
Un traitement prolongé est nécessaire pour réduire le risque de rechute, d’après des études rétrospectives réalisées dans des régions endémiques10. Pendant la phase initiale intensive, il est recommandé d’administrer de la ceftazidime ou du méropénem pendant 10–14 jours, voire plus; on peut aussi y associer du triméthoprime–sulfaméthoxazole en cas d’abcès ou d’atteinte osseuse, articulaire ou du système nerveux central. En outre, le drainage de l’abcès ou le débridement est crucial pour éradiquer le foyer infectieux initial. Ensuite, pendant la phase d’éradication, le triméthoprime–sulfaméthoxazole est recommandé pendant au moins 3 mois, et peut être prolongé à 6 mois en cas d’atteinte du système nerveux central ou d’ostéomyélite3. D’efficacité inférieure, l’amoxicilline–acide clavulanique ou la doxycycline peuvent être prescrites si le triméthoprime–sulfaméthoxazole est contre-indiqué5. Une récidive est possible chez 5 % des personnes, en raison d’une nouvelle infection, d’une éradication du foyer infectieux initial inadaptée ou d’un traitement intensif abrégé3,4.
Conclusion
La mélioïdose est une infection contractée dans les régions tropicales et subtropicales (y compris au sud des États-Unis), capable de se manifester après une longue latence. Les cliniciens devraient envisager cette infection chez les personnes ayant des antécédents de voyage pertinents et présentant un syndrome fébrile avec un abcès ou une atteinte articulaire.
La section Études de cas présente de brefs rapports de cas à partir desquels des leçons claires et pratiques peuvent être tirées. Les rapports portant sur des cas typiques de problèmes importants, mais rares ou sur des cas atypiques importants de problèmes courants sont privilégiés. Chaque article commence par la présentation du cas (500 mots maximum), laquelle est suivie d’une discussion sur l’affection sous-jacente (1000 mots maximum). La soumission d’éléments visuels (p. ex., tableaux des diagnostics différentiels, des caractéristiques cliniques ou de la méthode diagnostique) est encouragée. Le consentement des patients doit impérativement être obtenu pour la publication de leur cas. Renseignements destinés aux auteurs: www.cmaj.ca
Remerciements
Les auteurs sont reconnaissants au Dr Mark Downing pour les soins prodigués à cette patiente. Nous remercions la Dre Julianne Kus (laboratoire de Santé publique Ontario) et la section Élaboration d’épreuves et diagnostic — microbiologie médicolégale du Laboratoire national de microbiologie (Winnipeg, Manitoba) pour leur expertise technique.
Footnotes
Intérêts concurrents: Greg German déclare agir à titre de membre du conseil d’administration de Phage Canada (organisme sans but lucratif). Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement de la patiente.
Collaborateurs: Tous les auteurs ont contribué à l’élaboration et à la conception du travail. Mara Waters et Ellen Avery ont rédigé le manuscrit. Greg German, Sigmund Krajden et Yan Chen ont révisé de façon critique son contenu intellectuel important. Tous les auteurs ont donné leur approbation finale pour la version destinée à être publiée et endossent l’entière responsabilité de tous les aspects du travail.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/