Abstract
Contexte: Les différences d’immunogénicité entre les vaccins anti-SRAS-CoV-2 à ARNm n’ont pas été bien caractérisées chez les patients hémodialysés. Nous avons comparé la réponse sérologique chez les patients sous hémodialyse après la vaccination contre le SRAS-CoV-2 au moyen des vaccins BNT162b2 (Pfizer-BioNTech) et mRNA-1273 (Moderna).
Méthodes: Nous avons procédé à une étude de cohorte observationnelle et prospective dans 2 centres universitaires de Toronto, au Canada, du 2 février au 20 juillet 2021, et avons inclus 129 et 95 patients qui ont reçu respectivement les vaccins anti-SRAS-CoV-2 BNT162b2 et mRNA-1273. Nous avons mesuré les taux d’anticorps IgG dirigés contre la protéine S (anti-S), contre le domaine de liaison au récepteur (ou RBD, pour receptor-binding domain [anti-RBD]) et contre la protéine de la nucléocapside (anti-N) du SRAS-CoV-2 6–7) puis 12 semaines après la deuxième dose de vaccin et nous avons comparé ces taux aux taux médians d’anticorps présents dans le sérum de 211 témoins convalescents qui avaient déjà contracté le SRAS-CoV-2.
Résultats: Six à 7 semaines après la deuxième dose de vaccin, nous avons constaté que 51 patients sur 70 (73 %) ayant reçu le BNT162b2 et 83 patients sur 87 (95 %) ayant reçu le mRNA-1273, ont obtenu des taux équivalents à ceux du sérum de convalescents pour ce qui est de l’anticorps anti-S (p < 0,001). Chez ceux qui ont reçu le BNT162b2, 35 sur 70 (50 %) ont atteint le taux du sérum de convalescents pour l’anti-RBD, contre 69 sur 87 (79 %) de ceux qui ont reçu le mRNA-1273 (p < 0,001). Douze semaines après la deuxième dose, les taux d’anti-S et d’anti-RBD étaient significativement moindres chez les patients ayant reçu le BNT162b2 que chez ceux qui avaient reçu le mRNA-1273. Pour l’anti-S, 70 patients sur 122 (57,4 %) ayant reçu le BNT162b2 ont maintenu un taux équivalent à celui du sérum de convalescents, contre 68 sur 71 (96 %) de ceux qui avaient reçu le mRNA-1273 (p < 0,001). Pour l’anti-RBD, 47 patients sur 122 (38,5 %) ayant reçu le BNT162b2 ont maintenu des taux anti-RBD équivalant à celui du sérum de convalescents, contre 45 sur 71 (63 %) de ceux qui avaient reçu le mRNA-1273 (p = 0,002).
Interprétation: Chez les patients hémodialysés, le mRNA-1273 a généré une réponse humorale plus forte que le BNT162b2. Étant donné le déclin rapide de l’immunogénicité à 12 semaines chez les patients ayant reçu le BNT162b2, une troisième dose est recommandée chez les patients hémodialysés dans le cadre d’une première série, ce qui concorde avec les recommandations concernant d’autres populations vulnérables.
Les patients atteints d’insuffisance rénale au stade terminal qui sont hémodialysés sont exposés à un risque accru de contracter la forme grave de la COVID-19, les taux de mortalité variant de 9 % à 28 %1,2. Des vaccins hautement efficaces ont été développés contre le SRAS-CoV-2 et leur efficacité à réduire le risque de contracter la forme grave de la COVID-19 (souche D614G) est de 94,1 % à 95 %, comme l’ont confirmé 2 volumineux essais randomisés et contrôlés. Par contre, ces études incluaient peu d’insuffisants rénaux3,4. La réponse humorale à la vaccination semble hétérogène chez les patients dialysés comparativement à la population générale et une synthèse de 35 études sur des patients dialysés a révélé qu’au cours du mois suivant la deuxième dose de vaccin, les taux de séroconversion variaient de 70 % à 96 %5.
Les vaccins anti-SRAS-CoV-2 BNT162b2 (Pfizer BioNTech) et mRNA-1273 (Moderna) sont tous deux à base d’ARNm encapsulé dans des nanoparticules à nucléoside modifié encodant la protéine S du SRAS-CoV-2 pleine longueur stabilisée dans sa conformation préfusion. Le vaccin BNT162b2 est administré en doses de 30 μg à 21 jours d’intervalle et le vaccin mRNA-1273 est administré en doses de 100 μg à 28 jours d’intervalle3,4. La protéine S du SRAS-CoV-2 et son domaine de liaison au récepteur (ou RBD, pour receptor-binding domain) sont des antigènes ciblés par les vaccins actuellement commercialisés et sont utilisés pour mesurer la réponse humorale à la vaccination ou à l’infection naturelle. Une réponse immunitaire à la quantité de protéine de la nucléocapside (N), non ciblée par les vaccins anti-SRAS-CoV-2 à ARNm peut servir de marqueur d’une exposition naturelle au SRAS-CoV-2.
La reconnaissance de la morbidité et de la mortalité élevées liées à la COVID-19 et de l’immunogénicité réduite des vaccins anti-SRAS-CoV-2 chez les patients hémodialysés a permis de prioriser la vaccination chez cette population dans plusieurs régions1,6. Toutefois, les différences d’immunogénicité des vaccins anti-SRAS-CoV-2 n’ont pas été bien caractérisées chez cette population vulnérable. Nous avons donc réalisé une étude observationnelle et prospective auprès d’une cohorte de patients hémodialysés ayant reçu comme vaccin, soit le mRNA-1273, soit le BNT162b2, pour évaluer la réponse humorale en comparant les taux d’anticorps anti-S et anti-RBD après la deuxième dose de vaccin.
Méthodes
Conception de l’étude et participants
Nous avons réalisé une étude de cohorte observationnelle et prospective qui a inclus des patients de 18 ans ou plus hémodialysés (y compris des patients ayant déjà contracté la COVID-19 confirmée par test d’amplification en chaîne par polymérase couplée à une transcription inverse [RT-PCR]) pour évaluer la réponse immunitaire aux 2 vaccins anti-SRAS-CoV-2 à ARNm disponibles, dans 2 centres universitaires de Toronto en Ontario (Centre des sciences de la santé Sunnybrook et Réseau universitaire de santé). Le type de vaccin administré était spécifique aux centres: le BNT162b2 a été utilisé au Centre des sciences de la santé Sunnybrook et le mRNA-1273 a été utilisé au Réseau universitaire de santé. Les patients dialysés recevaient une hémodialyse en centre, une hémodialyse nocturne en centre ou une hémodialyse à domicile. Nous avons recruté 224 participants entre le 2 février et le 20 juillet 2021 dans les 2 centres. Nous avons obtenu un consentement éclairé écrit de tous les participants.
Analyses sérologiques
Nous avons mesuré les anticorps (IgG) anti-S, anti-RBD et anti-N du SRAS-CoV-2 à partir d’une plateforme automatisée de tests ELISA (enzyme-linked immunosorbent assay)7–9, comme rapporté précédemment, 6–7 semaines, puis 12 semaines après la deuxième dose de vaccin. Les taux d’anticorps ont été présentés sous forme de ratios relatifs par rapport à une norme déterminée avec courbe d’étalonnage pour chaque plaque multipuits. Nous avons utilisé VHH72-hFc1X7 (VHH-72-Fc) en tant que norme déterminée pour les anticorps anti-S et anti-RBD, comme décrit précédemment10, tandis que l’IgG humaine antinucléocapside (clone HC2003, GenScript, no A02039) a été utilisée pour l’anti-N. Pour VHH72-hFc1X7, l’anticorps monoclonal à domaine unique de lama VHH-72 a été exprimé sous forme de protéine de fusion Fc humaine: VHH-72-hFc1X7 (entrée no 6WAQ_1 de la PDB). Nous avons isolé d’autres VHH (NRCoV2–04 et NRCoV2–20) à l’interne à partir de lamas immunisés avec un ectodomaine recombinant de la protéine trimérique de spicule du SRAS-CoV-2 SmT1. Les séquences VHH ont été fusionnées avec un fragment Fc d’IgG1 humaine atténué, à cytotoxicité dépendante des anticorps et à médiation cellulaire (hFc1X7, brevet américain no 2019 352 383A1). Un tableau de conversion des ratios relatifs en unités standard internationales, ou BAU/mL, de l’Organisation mondiale de la Santé est fourni à l’annexe 1, accessible en anglais au: www.cmaj.ca/lookup/doi/10.1503/cmaj.211881/tab-related-content.
Nous avons déterminé les seuils de positivité (séroconversion) en regroupant les données des témoins négatifs et en calculant la moyenne plus 3 écarts-types (É.-T.). Les taux seuils de séroconversion ont été de 0,19, 0,186 et 0,396 pour les anticorps, anti-S, anti-RBD et anti-N, respectivement. Nous avons aussi comparé les taux d’anticorps aux taux médians dans le sérum de convalescents prélevé 21–115 jours après l’apparition des symptômes dans une cohorte de 211 patients de la population générale (âge médian 59 ans) qui présentaient une forme bénigne à grave de la COVID-19. Nous avons considéré le taux médian d’anticorps dans le sérum de convalescents comme une réponse immunitaire robuste11; les médianes étaient de 1,38, 1,25 et 1,13 pour les anticorps anti-S, anti-RBD et anti-N, respectivement.
Analyse statistique
Nous avons comparé les caractéristiques de référence des participants à l’aide d’un test t pour les variables continues et de tests exacts du χ2 ou de Fisher pour les variables catégoriques. Les taux d’anti-S et d’anti-RBD présentaient une distribution inégale et ont été comparés entre les patients sous BNT162b2 et mRNA-1273 à l’aide du test de Mann–Whitney. Pour les patients dont les résultats sérologiques étaient disponibles après 6–7 et 12 semaines, nous avons comparé les proportions à l’aide du test de McNemar. Pour tenir compte des écarts entre les caractéristiques de référence, les taux d’anti-S et d’anti-RBD à 6–7, puis à 12 semaines ont été transformés par la fonction y = [ratio relatif – min (ratio relatif) + 0,001] / [max (ratio relatif) – max (ratio relatif) + 0,002] à intégrer dans l’intervalle unité [0,1]. Nous avons utilisé les données transformées de β-régression avec la fonction de lien logit et les avons ajustées pour les covariables suivantes afin de fournir des estimations des ratios relatifs entre les 2 groupes étudiés: âge, sexe, immunosuppression, antécédents de transplantation d’organe plein, coronaropathie et diabète sucré. Nous avons choisi les covariables selon les facteurs susceptibles d’affecter l’immunogénicité ou selon l’écart entre les deux groupes. La β-régression est un modèle linéaire généralisé qui fournit des estimations pour les variables dépendantes tout en modélisant les changements des variances sous forme de paramètres moyens et de précision, et permet de modéliser les variables ne suivant pas une distribution normale. Nous avons évalué les hypothèses pour le modèle de régression à partir de l’analyse des résidus standardisés, la multicolinéarité à l’aide du test de Fisher pour les variables binaires, et la régression linéaire simple pour les variables continues. Nous avons utilisé la fonction de liaison logit pour obtenir les estimations des paramètres pour les effets des covariables sur les taux d’anticorps transformés. Nous avons calculé les rapports des cotes (RC) par exponentiation des estimations des paramètres pour déterminer la solidité du lien entre un changement des variables explicatives, notamment le type de vaccin et les taux d’anti-S ou d’anti-RBD. Toutes les covariables étaient binaires sauf l’âge, qui était continu. Nous avons effectué l’amorçage avec 5000 réplications pour calculer les intervalles de confiance (IC) de 95 % pour la différence médiane des taux d’anti-S et d’anti-RBD à 6–7 semaines et à 12 semaines. Nous avons considéré qu’une valeur p bilatérale de 0,05 était significative. Nous avons effectué toutes les analyses au moyen de la version R 3.6.1 (gratuiciel R de calcul statistique).
Approbation éthique
L’étude a été approuvée par l’Hôpital Mont-Sinaï, le Centre des sciences de la santé Sunnybrook et le Réseau universitaire de santé (CTO no 3604).
Résultats
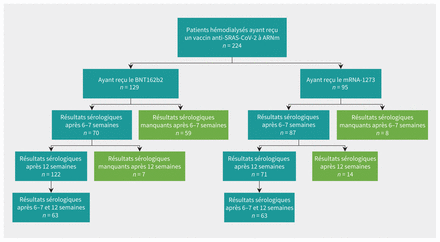
Parmi les 224 patients dialysés, 129 ont reçu le BNT162b2 et 95 ont reçu le mRNA-1273. Aucun effet indésirable grave n’a été signalé avec l’un ou l’autre des vaccins chez aucun des participants. Parmi ceux qui ont reçu le BNT162b2, 70 ont subi des analyses sérologiques aux semaines 6–7, et 122 à la semaine 12 après la deuxième dose de vaccin (figure 1); ces patients avaient un âge médian de 72 ans (écart interquartile [ÉI] 62–79), 41 sur 129 (31,7 %) étaient de sexe féminin et 6 sur 129 (4,6 %) avaient déjà contracté la COVID-19, confirmée par RT–PCR. Parmi ceux qui avaient reçu le mRNA-1273, 87 ont subi des analyses sérologiques aux semaines 6–7, et 71 à la semaine 12 après la deuxième dose de vaccin; ces patients avaient un âge médian de 62 ans (ÉI 55–67), 25 sur 95 (26 %) étaient de sexe féminin et 5 sur 95 (5,3 %) avaient déjà contracté le SRAS-CoV-2. Les patients ayant reçu le BNT162b2 étaient plus nombreux à souffrir de diabète sucré et de coronaropathie, tandis qu’une proportion plus élevée de patients ayant reçu le mRNA-1273 avaient des antécédents de transplantation d’organe plein et prenaient des immunosuppresseurs (tableau 1). Nous avons constaté que les signes sérologiques d’une exposition antérieure au SRAS-CoV-2, anti-N-séropositivité à l’appui, étaient similaires entre les groupes: 10 sur 87 (12 %) ayant reçu le mRNA-1273 et 12 sur 70 (17 %) ayant reçu le BNT162b2 étaient séropositifs à l’égard des anticorps anti-N aux semaines 6–7 (p = 0,3) et 4 sur 71 (6 %) ayant reçu le mRNA-1273 et 14 sur 122 (11,5 %) ayant reçu le BNT162b2 étaient séropositifs à l’égard de l’anti-N 12 semaines après la vaccination (p = 0,2) (tableau 2).
Diagramme des cohortes de patients hémodialysés de l’étude entre le 2 février et le 20 juillet 2021, qui ont été vaccinées contre le SRAS-CoV-2 avec 2 doses de BNT162b2 (Pfizer-BioNTech) ou de mRNA-1273 (Moderna), et moment de l’évaluation sérologique du SRAS-CoV-2 après la deuxième dose de vaccin. À noter: Des résultats sérologiques sont manquants pour les patients ayant reçu le BNT162b2 (n = 59) à 6–7 semaines en raison du moment du début de l’étude qui a fait en sorte que des échantillons de référence ont été omis à ce site. D’autres lacunes dans les résultats sérologiques sont le reflet de séances d’hémodialyse prévues qui ont été manquées dans la population dialysée, ou d’hospitalisations intercurrentes.
Caractéristiques des patients hémodialysés ayant reçu les vaccins BNT162b2 et mRNA-1273 contre le SRAS-CoV-2
Ratios relatifs, séroconversion et proportion de patients ayant atteint les taux médians de sérum de convalescents pour les anticorps anti-SRAS-CoV-2 après vaccination par BNT162b2 ou mRNA-1273
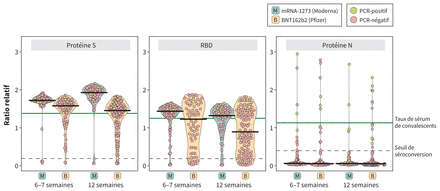
Six à 7 semaines après la deuxième dose de vaccin, nous avons constaté des taux médians d’anti-S significativement plus élevés avec le mRNA-1273 (ratio relatif médian de 1,72, ÉI 1,68–1,79) qu’avec le BNT162b2 (ratio relatif médian de 1,58, ÉI 1,28–1,67; p < 0,001). Nous n’avons observé aucune différence significative quant aux taux d’anti-RBD (ratio relatif médian de 1,44, ÉI 1,29–1,53, avec le mRNA-1273 et ratio relatif médian de 1,23, ÉI 0,61–1,64 avec le BNT162b2; p = 0,2). En utilisant les taux sériques médians du sérum de convalescents comme marqueur d’une réponse immunitaire robuste chez les individus ayant reçu le mRNA-1273, 83 sur 87 (95 %) présentaient des taux d’anti-S et 69 sur 87 (79 %) présentaient des taux d’anti-RBD semblables à ceux du sérum de convalescents, 6–7 semaines après la vaccination. Cela s’est révélé supérieur aux effets du BNT162b2 avec lequel 51 sur 70 (73 %) ont présenté des taux d’anti-S et 35 sur 70 (50 %) des taux d’anti-RBD semblables à ceux du sérum de convalescents (p < 0.001) (tableau 2).
Douze semaines après la deuxième dose de vaccin, les taux d’anti-S avaient décliné comparativement au taux après 6–7 semaines suivant la deuxième dose de vaccin chez ceux qui avaient reçu le BNT162b2, mais non chez ceux qui avaient reçu le mRNA-1273 (p < 0.001). Les taux d’anti-S à 12 semaines sont restés plus bas chez les patients ayant reçu le BNT162b2 (ratio relatif médian de 1,45, ÉI 1,09–1,58) que chez ceux qui avaient reçu le mRNA-1273 (ratio relatif médian de 1,93, ÉI 1,76–2,02; p < 0,001). De même, les taux d’anti-RBD étaient plus bas chez les patients ayant reçu le BNT162b2 (ratio relatif médian de 0,89, ÉI 0,36–1,43) que chez ceux qui avaient reçu le mRNA-273 (ratio relatif médian de 1,32, ÉI 1,04–1,47; p = 0,002) à 12 semaines (figure 2). Correspondant au déclin des taux d’anti-S et d’anti-RBD, 70 patients sur 122 (57,4 %) ayant reçu le BNT162b2 avaient des taux d’anticorps supérieurs aux taux médians d’anti-S du sérum de convalescents, contre 68 sur 71 (96 %) ayant reçu le mRNA-1273 (p < 0,001) à 12 semaines. À 12 semaines, 47 patients sur 122 (38,5 %) ayant reçu le BNT162b2 ont dépassé le taux médian d’anti-RBD du sérum de convalescents comparativement à 45 patients sur 71 (63 %) ayant reçu le mRNA-1273 (p = 0,002). Trois patients ayant reçu le BNT162b2 avaient une infection au SRAS-CoV-2 confirmée par RT–PCR, 4, 11 et 81 jours après la deuxième dose de vaccin et 2 de ces patients ont dû être hospitalisés. Aucun patient ayant reçu le mRNA-1273 n’a contracté la COVID-19 durant la période de l’étude.
Réponse des anticorps anti-S, anti-RBD et anti-N à l’IgG du SRAS-CoV-2 chez des patients hémodialysés après vaccination par mRNA-1273 (Moderna; n = 95) ou BNT162b2 (Pfizer-BioNTech; n = 129). Le pointillé représente les échantillons sériques individuels recueillis 6–7 semaines et 12 semaines suivant la 2e vaccination. Les patients ayant déjà contracté le SRAS-CoV-2 confirmé par RT–PCR sont indiqués en vert. Les taux d’anticorps sont représentés sous forme de ratios relatifs par rapport à des normes déterminées. Les taux seuil de séroconversion représentent un test positif et sont de 0.19, 0.186 et 0.396 pour les anticorps anti-S, anti-RBD et anti-N, respectivement, et sont indiqués par la ligne hachurée pour chaque anticorps. Les taux d’anticorps médians pour chaque antigène sont indiqués par des lignes noires continues. Le taux médian d’antigène dans le sérum de convalescents provient d’une cohorte de 211 patients de la population générale ayant contracté la COVID-19, peu importe la gravité, et représente une réponse immunitaire robuste (1.38, 1.25 et 1.13 pour les anticorps anti-S, anti-RBD et anti-N, respectivement) comme l’indique la ligne verte de chaque anticorps. Remarque: PN = protéine de la nucléocapside, RBD = domaine de liaison au récepteur, RT–PCR = test d’amplification en chaîne par polymérase couplée à une transcription inverse.
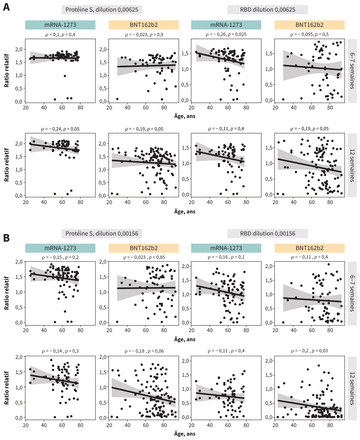
Nous avons réalisé une analyse longitudinale des patients dont les résultats sérologiques (n = 126) 6–7 puis 12 semaines après la deuxième dose de vaccin confirmaient une immunogénicité plus marquée avec le mRNA-1273 qu’avec le BNT162b2 (annexe 2, accessible en anglais ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.211881/tab-related-content), même si l’écart persistait pour un certain nombre de caractéristiques de référence (annexe 3, accessible en anglais ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.211881/tab-related-content). Nos résultats sont restés similaires après avoir exclu de l’analyse les patients ayant des antécédents de COVID-19 confirmée par RT–PCR ou d’anti-N-séroconversion durant la période de l’étude (annexes 4 et 5, accessibles en anglais ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.211881/tab-related-content), après une analyse séparée des patients qui prenaient des immunosuppresseurs ou qui avaient des antécédents de transplantation d’organe plein (annexe 6, accessible en anglais ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.211881/tab-related-content) et après comparaison selon l’âge (figure 3). Les résidus standardisés de Pearson dans les modèles de β-régression étaient comme prévu centrés autour du 0, ce qui confirme la relation linéaire entre les covariables et les taux d’anticorps (annexe 7, accessible en anglais ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.211881/tab-related-content). Six à 7 semaines après la vaccination, nous avons constaté que le mRNA-1273 était associé à des taux plus élevés d’anti-S (RC non ajusté 1,79, IC de 95 % 1,30–2,47; RC ajusté 2,04, IC de 95 % 1,39–3,01), tandis que les taux d’anti-RBD n’ont pas été significativement plus élevés (RC non ajusté 1,15, IC de 95 % 0,81–1,63; RC ajusté 1,44, IC de 95 % 0,96–2,16) qu’avec le BNT162b2 (tableau 3). Cela s’est accentué à 12 semaines: le mRNA-1273 a été associé à des taux plus élevés d’anti-S (RC non ajusté 2,94, IC de 95 % 2,17–3,97; RC ajusté 3,34, IC de 95 % 2,42–4,62) et d’anti-RBD (RC non ajusté 1,46, IC de 95 % 1,05–2,03; RC ajusté 1,55, IC de 95 % 1,09–2,21). Nous avons confirmé les taux plus élevés d’anti-S et d’anti-RBD avec le mRNA-1273 au moyen d’un amorçage avec 5000 réplications (annexes 8 et 9, accessibles en anglais ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.211881/tab-related-content).
Réponse des anticorps anti-S et anti-RBD chez des patients hémodialysés après vaccination par mRNA-1273 (Moderna; n = 95) ou BNT162b2 (Pfizer-BioNTech; n = 129), selon l’âge. Les résultats sont montrés pour les niveaux de dilution (A) 0,00625 et (B) 0,00156. Les lignes de régression linéaire avec intervalle de confiance de 95 % (en gris) sont présentées avec les valeurs ρ et p de Spearman correspondantes. Le pointillé représente les échantillons sériques individuels recueillis 6–7 semaines et 12 semaines suivant la deuxième vaccination. Les taux d’anticorps sont représentés sous forme de ratios relatifs par rapport à des normes déterminées. Les taux seuils de séroconversion représentent un test positif et sont de 0,19 et 0,186 pour les anticorps anti-S et anti-RBD, respectivement. Remarque: RBD = domaine de liaison au récepteur.
Modèles de β-régression multivariée pour les prédicteurs des taux d’anti-S ou d’anti-RBD 6–7 semaines et 12 semaines après la deuxième dose de vaccin
Interprétation
Nous avons comparé la réponse humorale après la vaccination contre le SRAS-CoV-2 chez 224 patients hémodialysés et constaté que le mRNA-1273 générait une immunogénicité supérieure à celle du BNT162b2 6–7 semaines après la vaccination et les taux d’anticorps se maintenaient mieux avec le mRNA-1273 à 12 semaines. Même si nous avons mesuré uniquement la réponse sérologique à la vaccination, une réponse humorale est nécessaire pour obtenir une réponse cellulaire adéquate12,13. Le déclin des anticorps anti-SRAS-CoV-2 12 semaines après la vaccination chez ceux qui ont reçu le BNT162b2 est préoccupant puisque les taux d’anti-S et d’anti-RBD sont généralement en corrélation avec les taux d’anticorps neutralisants qui, nous l’inférons, protégeraient contre une infection à SRAS-CoV-2 symptomatique11. Nos résultats concordent avec ceux d’une étude regroupant 2367 patients hémodialysés aux Etats-Unis, 28–60 jours après la vaccination: 22,7 % de ceux qui ont reçu le BNT162b2 n’avaient aucun taux détectable d’IgG anti-RBD, contre 9,4 % de ceux qui avaient reçu le mRNA-1273 (taux mesurés à l’aide d’un test commercial semi-quantitatif)14.
Les évaluations des différences d’immunogénicité entre les vaccins à ARNm sont limitées. Une étude de 2021 regroupant 1647 travailleurs de la santé en Belgique a observé que les taux d’anti-S du SRAS-CoV-2 étaient significativement plus élevés avec le mRNA-1273 qu’avec le BNT162b2 6–10 semaines après la deuxième dose de vaccin15. Selon les auteurs, cette différence pourrait être attribuable à la teneur plus élevée en ARNm du mRNA-1273 et à la période de rappel légèrement plus longue (28 c. 21 j)15. Une étude de 2021 sur des résidents et des travailleurs de la santé d’établissements de soins de longue durée en Ontario a fait état d’une réponse humorale plus forte avec le mRNA-1273 qu’avec le BNT162b216. Les résidents d’établissements de soins de longue durée qui ont reçu le BNT162b2 ont produit 3,89 fois moins d’anticorps neutralisants contre la souche sauvage D614G du SRAS-CoV-2 selon un dosage de lentivirus pseudotypé à protéine S, comparativement à ceux qui avaient reçu le mRNA-1273, et ce taux a diminué encore selon un facteur de 4,25 contre le variant B.1.617.2 (Delta)16.
Un déclin des taux d’anticorps a été observé dans la population générale, en particulier chez les personnes qui avaient reçu 2 doses de BNT162b2 après l’intervalle suggéré de 21 jours. Par exemple, lors d’une étude menée en 2021 en Israël, un déclin des titres d’anticorps après la vaccination anti-SRAS-CoV-2 a révélé que 16,1 % des personnes vaccinées 2 fois avec le BNT162b2 présentaient des taux d’anti-S inférieurs aux seuils de séropositivité à 6 mois17. Il a été démontré que les doses de rappel chez les adultes âgés réduisaient le risque d’infection postvaccinale au SRAS-CoV-2 dans cette population18 et sont par conséquent recommandées au Canada pour toute personne de plus de 18 ans. Chez les personnes ayant subi une transplantation d’organe, une troisième dose de vaccin a aussi réussi à améliorer l’immunogénicité, ce qui a mené à l’approbation à grande échelle des séries de 3 doses chez les receveurs de transplantation d’organes pleins au Canada19.
Les patients hémodialysés présentent une réponse humorale altérée comparativement aux témoins en bonne santé et ont souvent besoin de doses de rappel dans le contexte de la vaccination contre l’hépatite B. Étant donné l’immunogénicité postvaccinale réduite et un risque élevé de contracter une forme grave de la COVID-19, les patients hémodialysés en France, en Israël et aux Etats-Unis ont reçu d’emblée une troisième dose de vaccin anti-SRAS-CoV-2 qui a amélioré la réponse humorale, surtout chez ceux qui avaient moins bien répondu à 2 doses de vaccin20,21. Dans une étude observationnelle et prospective de 2021 réalisée en France sur une cohorte de patients hémodialysés, une troisième dose de BNT162b2 a donné lieu à une séroconversion chez plus de la moitié des patients qui étaient restés séronégatifs après 2 doses22. Au Canada, une troisième dose de vaccin à ARNm anti-SRAS-CoV-2 a été approuvée pour les patients dialysés. En Ontario, 74 % des patients hémodialysés vaccinés ont reçu le BNT162b2, ce qui suscite des préoccupations en raison de la baisse rapide de l’immunogénicité à 12 semaines chez les patients ayant reçu le BNT162b2 dans notre étude. En outre, les unités d’hémodialyse sont exposées à un risque d’éclosion de COVID-19 en raison de la difficulté d’y appliquer les règles de distanciation physique, et des infections postvaccinales ont été décrites chez des patients hémodialysés dont les titres d’anticorps étaient bas23,24. Même si nous avons observé 3 cas de COVID-19 après une deuxième dose de vaccin uniquement dans le groupe sous BNT162b2 dans notre étude, 2 de ces cas sont survenus moins de 14 jours après la deuxième dose et les infections postvaccinales doivent faire l’objet d’études plus approfondies. Toutefois, une étude américaine de 2021 sur 56 infections postvaccinales chez des patients hémodialysés a révélé que ceux dont les taux d’IgG anti-RBD étaient inférieurs à 218 BAU/mL étaient 11,6 fois plus à risque à l’égard des infections postvaccinales25.
Les données concrètes viennent étayer les différences potentielles d’efficacité entre les vaccins anti-SRAS-CoV-2 à ARNm. Une grande étude observationnelle menée dans le réseau de services médicaux de la clinique Mayo regroupant une cohorte de patients vaccinés appariés a révélé que même si l’efficacité du mRNA-1273 était similaire à celle du BNT162b2 au début de 2021, après l’émergence du variant B.1.617.2 (Delta) en juillet 2021, la vaccination par mRNA-1273 a conféré une réduction 2 fois plus grande du risque d’infection postvaccinale comparativement au BNT162b226. D’autres études de population seront nécessaires pour confirmer que les différences d’immunogénicité correspondent à une baisse de l’efficacité des vaccins, mais en attendant de telles données, l’immunogénicité a déjà été utilisée pour orienter les prises de décision en matière de vaccination dans d’autres groupes à risque, notamment les adultes âgés et les receveurs de transplantation d’organes.
Limites de l’étude
Notre étude a été limitée par son protocole observationnel, qui a donné lieu à des différences dans plusieurs caractéristiques de référence entre les 2 cohortes, et par la taille de l’échantillon basée sur un échantillonnage de commodité durant la période de l’étude. Toutefois, après ajustement pour tenir compte de variables de confusion potentielles avec une analyse de régression, le constat de l’immunogénicité supérieure du mRNA-1273 comparé au BNT162b2 a persisté. Les patients ayant reçu le BNT162b2 dans notre étude étaient plus âgés, ce qui témoigne d’un début plus précoce de l’étude lorsque les patients âgés étaient priorisés pour la vaccination. Cela a été contrebalancé par l’utilisation d’immunosuppresseurs chez les receveurs du mRNA-1273, associée à des taux moindres d’anticorps. Même si les taux d’anticorps sont un marqueur utile de l’immunogénicité11 et même s’il a été démontré qu’ils sont en corrélation avec une réduction des formes graves d’infection au SRAS-CoV-227, le taux d’anticorps requis pour une protection contre la COVID-19 reste à déterminer28,29. De plus, la définition d’une immunité robuste dans le cadre de notre étude a servi de marqueur substitut défini comme l’atteinte du taux d’anticorps médian du sérum de convalescents. Même si le sérum de convalescents peut être un comparateur utile, des études de longue durée seront nécessaires pour en confirmer la valeur et la corrélation avec l’efficacité des vaccins.
Conclusion
Nous avons constaté une immunogénicité plus grande avec le vaccin mRNA-1273 qu’avec le vaccin BNT162b2 chez des patients hémodialysés, avec un déclin rapide de l’immunogénicité 12 semaines après la deuxième dose de vaccin chez les patients ayant reçu le BNT162b2. À la lumière de ces observations, une troisième dose rapprochée de vaccin anti-SRAS-CoV-2 est recommandée chez cette population vulnérable.
Remerciements
Les dosages d’anticorps et l’analyse initiale des données ont été effectués par Bhavisha Rathod, Mahya Fazel-Zarandi, Jenny Wang et Adrian Pasculescu. Nous avons obtenu les données sur le sérum de convalescents du Toronto Invasive Bacterial Diseases Network (études REB no 20-044, Unity Health; no 02-0118-U/05-0016-C, Hôpital Mont-Sinai).
Footnotes
Intérêts concurrents: Mohammad Atiquzzaman et Adeera Levein sont des employés de la BC Renal Agency. Matthew Oliver et Michelle Hladunewich sont des cadres médicaux contractuels du Réseau rénal Ontario, de Santé Ontario. Matthew Oliver est propriétaire d’Oliver Medical Management Inc., qui distribue sous licence des logiciels d’analyse pour la gestion de la dialyse et la préparation de rapports. Il détient un brevet canadien pour le système DMAR, il a reçu des honoraires de conférencier de Baxter Healthcare et a participé à des comités consultatifs pour Janssen et Amgen. Jeffrey Perl a reçu des honoraires de consultation de Baxter Healthcare, US Renal Care, Davita Healthcare Partners, Otsuka Canada et AstraZeneca Canada, indépendamment des travaux soumis; des subventions de l’Agency for Healthcare Research and Quality grant support; et des honoraires de consultation de Baxter Healthcare, Fresenius Medical Care USA, AstraZeneca, Davita Healthcare Partners et US Renal Care. Shelly Bolotin a reçu des subventions des Instituts de recherche en santé du Canada (IRSC), du Réseau canadien de recherche sur l’immunisation, du Groupe de travail sur l’immunité face à la COVID-19 et de l’Agence de la santé publique du Canada, indépendamment des présents travaux. Elle est membre des comités directeurs du Réseau canadien de recherche sur l’immunisation et du Groupe de travail sur l’immunité face à la COVID-19. Vanessa Tran signale que Santé publique Ontario a reçu du financement de l’Agence de la santé publique du Canada et des trousses de dépistage des études de sérosurveillance du Groupe de travail sur l’immunité face à la COVID-19. Santé publique Ontario a aussi participé à un essai clinique de combinaison de vaccins contre la COVID-19. Shelly Bolotin et Vanessa Tran sont des employées de Santé publique Ontario. Adeera Levin est responsable des Réseaux cliniques et académiques intégrés pour Providence Health Care. Elle a participé à des comités du National Institute of Diabetes and Digestive and Kidney Diseases, des National Institutes of Health et de l’Australian Kidney Clinical Trials Network. Elle a un rôle de responsable ou de fiduciaire pour l’International Society of Nephrology (ISN) Advocacy Group, l’ISN International CKDu Consortium, l’ISN Research Committee et de la BC Renal Agency. Elle a reçu des honoraires de GSK, Takeda, Reata, AstraZeneca et Janssen; et des paiements pour un rôle de témoin expert d’Osler. Peter Blake est le directeur médical du Réseau rénal Ontario, Santé Ontario, et il a reçu des honoraires de conférencier de Baxter Global. Anne-Claude Gingras est membre d’équipes spéciales (dépistage et immunologie) du Groupe de travail sur l’immunité face à la COVID-19, elle est présidente du Comité consultatif de l’Institut de génétique des IRSC, elle est membre du Conseil national de recherche du Canada, membre du Conseil d’administration du Centre de recherche en thérapeutiques en santé humaine du Conseil national de recherche Canada; elle est responsable du volet Functional Genomics and Structure-Function pour CoVaRR-Net. Michelle Hladunewich a reçu des subventions de Pfizer, Ionis, Chemocentryx, Calliditas et Roche; des honoraires de consultation d’Alynylam; et des redevances de UpToDate, indépendamment des travaux soumis. Jerome Leis a reçu une rémunération en tant que témoin-expert de l’Association des hôpitaux de l’Ontario et du ministère du procureur général de l’Ontario et il occupe un poste de responsabilité au sein de la campagne Choisir avec soins. Kevin Yau a reçu des honoraires de conférencier d’AstraZeneca. Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Collaborateurs: Christopher Chan, Anne-Claude Gingras et Michelle Hladunewich sont les auteurs-superviseurs principaux. Kevin Yau et Kento Abe ont contribué également en tant que co-auteurs principaux. Kevin Yau, Christopher Chan, Jeffrey Perl, Shelly Bolotin, Vanessa Tran, Anne-Claude Gingras et Michelle Hladunewich ont contribué à la conception et à la modélisation du travail. Tous les auteurs ont contribué à l’acquisition, à l’analyse et à l’interprétation des données. Kevin Yau, Christopher Chan, Kento Abe, Anne-Claude Gingras et Michelle Hladunewich ont rédigé l’ébauche du manuscrit. Tous les auteurs ont révisé de façon critique le contenu intellectuel important du manuscrit; ils ont donné leur approbation finale pour la version destinée à être publiée et assument l’entière responsabilité de tous les aspects du travail.
Financement: L’étude a bénéficié du soutien du Groupe de travail sur l’immunité face à la COVID-19 (subvention no 2122-HQ-000071), financé par le gouvernement du Canada, et la bourse Oreopoulos/Baxter pour la dialyse à domicile de la Division néphrologie de l’Université de Toronto. L’équipement utilisé relève du Network Biology Collaborative Centre à l’Institut de recherche Lunenfeld-Tanenbaum, un établissement qui bénéficie du soutien financier de la Fondation canadienne pour l’innovation (no CFI 33474), du gouvernement de l’Ontario, de Génome Canada et de l’Institut de génomique de l’Ontario (OGI-139). Anne-Claude Gingras bénéficie de l’appui des Instituts de recherche en santé du Canada (IRSC; FDN 143301) et détient une chaire de recherche Canada (de niveau 1) en protéomique fonctionnelle. Elle a reçu une subvention de Providence Therapeutics, des IRSC (pour les études sur le SRAS-CoV-2) et du Fonds ontarien de recherche pour l’intervention rapide contre la COVID-19. Karen Colwill a fourni son assistance pour l’accord et géré le financement de Medivolve pour le développement initial d’un test ELISA (enzyme-linked immunosorbent assay) au Sinai Health System, indépendamment des travaux soumis. Adeera Levin a reçu un soutien d’AstraZeneca, Certa, Otsuka, Reata, Retrophin, du George Institute, de Boeingher Ingelehem, des IRSC, de Janssen, de la Fondation canadienne du rein, de Merck, des Oxford Clinical Trials, de Merck, Amgen et Bayer, des National Institutes of Health, du National Institute of Diabetes and Digestive and Kidney Diseases, de Chinook Therapeutics, et de Johnson et Johnson.
Partage des données: Les données anonymisées sont disponibles en tout ou en partie après demande raisonnable adressée à l’auteur-ressource, Michelle Hladunewich (michelle.hladunewich{at}sunnybrook.ca).
- Accepted January 10, 2022.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/